Banyak jurusan kuliah baru yang bermunculan seiring berkembangnya zaman. Kira-kira jurusan kuliah yang peluang kerjanya banyak apa saja?
Bingung Mau lanjut Kuliah Jurusan Apa? Ini 6 Jurusan Sesuai Hobi yang Bisa Kamu Pilih
Menentukan jurusan kuliah menjadi part tersulit bagi yang belum tau mau ambil jurusan apa. Yuk coba jurusan sesuai hobi kamu!
3 Prodi Baru ITS Ini Dibuka di SNBT 2024, Anak IT Wajib Simak!
Institut Teknologi Sepuluh Nopember Surabaya membuka 3 program studi baru yang bisa diikuti dari jalur SNBP dan SNBT. Cek selengkapnya disini!
Kenalan dengan Program IUP Telkom University, Pendaftarannya Sudah Dibuka!
Telkom University membuka program IUP dan pendaftarannya dimulai pada 22 Maret 2024 kemarin. Intip program studinya!
5 Rekomendasi Jurusan yang Berpeluang Jadi PNS, Ada Jurusanmu?
Profesi PNS menjadi idaman yang masih banyak diincar masyarakat Indonesia. Tapi ada 5 jurusan yang berpeluang jadi PNS lebih besar, lho!
Pengertian, Perkembangan dan Ragam Penemu Teori Atom
Dalam ilmu fisika dan kimia, Teori Atom merupakan salah satu teori yang digunakan untuk mengenali sifat dari sebuah benda. Teori ini menyatakan bahwa seluruh benda yang ada di dunia ini terbentuk dari adanya atom-atom yang saling menyatu. Tentu, teori ini bisa diterapkan untuk berbagai jenis benda, termasuk benda padat, benda cair dan benda gas.
Menurut pengertiannya, atom sendiri berasal dari kata dalam bahasa Yunani yang memiliki arti tidak bisa dibagi. Secara tidak langsung, arti dari kata atom ini merupakan sesuatu yang sangat kecil di mana tidak dimungkinkan untuk memisahkan atau membaginya lagi menjadi beberapa bagian.
Asal Usul Teori Atom
Dalam catatan sejarah, Teori Atom termasuk salah satu teori tertua yang muncul dan ditemukan di dunia. Teori ini kemudian dikembangkan menjadi lebih kompleks dan menjadi salah satu dasar pengetahuan yang cukup penting, terutama dalam sains. Menurut sejarah yang tercatat, penemu Teori Atom adalah seorang yang berasal dari Yunani, yakni Democritus.
Democritus merupakan tokoh ulung terkait Teori Atom. Ia merupakan seseorang yang pertama kali menemukan teori ini pada awal abad ke-5 sebelum masehi. Dalam hal ini, Democritus mengemukakan bahwa benda-benda yang ada bisa dibagi menjadi beberapa atau banyak bagian yang sangat kecil.
Bagian-bagian benda tersebut akhirnya tidak akan bisa dibagi lagi. Bagian inilah yang kemudian oleh Democritus disebut sebagai atom. Menurutnya, atom sepenuhnya padat, tidak terdapat struktur internal serta ada ruang kosong antar atom guna memberikan ruang untuk pergerakannya. Ia mencontohkan dengan pergerakan dalam air dan udara.
Selain itu, dalam penjelasan mengenai Teori Atom yang ia temukan, Democritus mengatakan bahwa ada perbedaan sifat dari material yang berbeda, atom memiliki perbedaan dan dibedakan dalam beberapa bentuk, massa serta ukurannya. Berdasarkan pada model atom yang ia buat, Democritus mampu menjelaskan jika memang atom-lah yang menyusun benda-benda.
Kemunculan teori ini menjadi salah satu tonggak pengetahuan yang penting dan memberikan perbedaan yang cukup signifikan. Dalam perkembangannya, Teori Atom ini kemudian dinamakan Teori Atom Democritus sesuai dengan nama penemunya.
Pengertian Struktur Atom
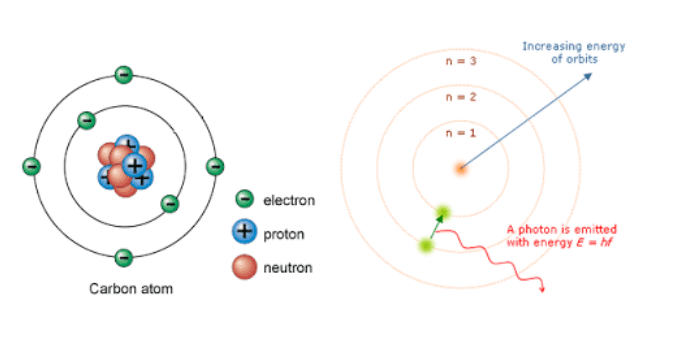
Perbincangan mengenai Teori Atom tidak bisa dilepaskan dari pembahasan mengenai struktur atom. Dalam pembahasannya, struktur atom merupakan satuan dasar materi di mana terdiri dari inti atom beserta awan elektron yang bermuatan negatif serta mengelilinginya. Inti dari atom tersebut memiliki kandungan campuran.
Campuran yang terdapat dalam inti dari atom adalah kandungan proton yang bermuatan positif dan juga neutron yang bermuatan netral. Elektron yang mengelilingi inti atom tersebut terikat dikarenakan dengan adanya gaya elektromagnetik. Tidak hanya itu, sekumpulan atom juga akan terikat dengan gaya yang sama dengan atom lain hingga nantinya akan membentuk molekul.
Oleh karena itu, dalam pembahasan mengenai Teori Atom, gaya elektromagnetik merupakan hal yang penting untuk dibahas dan memiliki pengaruh yang sangat besar. Struktur atom ini juga mengalami perkembangan dari waktu ke waktu hingga dibahas lebih detail.
Perkembangan Teori Atom
Seiring waktu berjalan, Teori Atom juga mengalami beberapa perkembangan yang cukup signifikan. Hal ini dikarenakan teori yang lama akan menyempurnakan teori sebelumnya. Salah satu fakta yang tercatat dalam penemuan teori ini oleh Democritus adalah ia kurang memiliki bukti eksperimental sehingga teorinya dianggap kurang sempurna.
Akhirnya, pada medio tahun 1800 mulai ditemukan beberapa penemuan baru terkait Teori Atom yang kehadirannya memberikan pengertian dan pemahaman yang luas mengenai apa itu atom. Pada masanya, terdapat beberapa perkembangan terkait teori ini yang datang dari beberapa tokoh yang berbeda.
Adapun tokoh-tokoh yang berperan penting mengenai muncul dan berkembangnya Teori Atom hingga saat ini adalah sebagai berikut:
1. Teori Atom Dalton
Perkembangan mengenai Teori Atom diawali oleh John Dalton. Ia mengemukakan pendapat awalnya mengenai atom pada tahun 1803. Dalam hal ini, teori yang dikemukakan oleh Dalton didasarkan pada dua hukum, yaitu hukum kekekalan massa atau hukum Lavoisier dan hukum susunan tetap atau hukum Proust.
Dalam penjelasannya, Lavoisier mengatakan bahwa massa total dari zat-zat sebelum reaksi akan selalu sama dengan massa total dari zat-zat yang dihasilkan dari reaksi. Sedangkan Proust mengatakan bahwa perbandingan massa pada unsur-unsur dalam suatu senyawa senantiasa akan selalu tetap.
Dari kedua hukum tersebut, John Dalton mengemukakan pendapatnya terkait Teori Atom sebagai berikut:
- Atom merupakan bagian terkecil dari sebuah materi dan karena ukurannya yang paling kecil sehingga tidak bisa lagi dibagi menjadi bagian lain.
- Atom digambarkan dengan bola pejal yang sangat kecil dengan kesimpulan bahwa suatu unsur memiliki atom-atom yang identik dan berbeda untuk unsur yang berbeda pula.
- Atom-atom bergabung untuk membentuk sebuah senyawa dengan perbandingan bilangan bulat serta sederhana. Dalam hal ini dimisalkan air yang terdiri dari atom-atom hidrogen dan atom-atom oksigen.
- Reaksi kimia merupakan pemisahan dan juga penggabungan atau penyusunan kembali dari rangkai atom-atom sehingga atom tidak akan bisa diciptakan atau dimusnahkan.
Pendapat dari Dalton ini menjadi awal dari perkembangan Teori Atom dalam dunia pengetahuan. Kemunculan teori Dalton ini juga memberikan beberapa kelebihan dalam pengetahuan yakni mulai membangkitkan minat terkait penelitian mengenai beragam jenis modal atom.
Akan tetapi, Teori Atom yang dikemukakan oleh Dalton masih memiliki beberapa kelemahan. Adapun beberapa kelemahan dari teori Dalton adalah sebagai berikut:
- Tidak dapat menjelaskan bagaimana cara atom tersebut saling berkaitan
- Tidak dapat menjelaskan hubungan antara larutan senyawa dengan daya hantar sebuah arus listrik karena atom merupakan bagian terkecil unsur atau benda yang tidak bisa dibagi lagi
- Tidak dapat menjelaskan sifat listrik materi
- Tidak bisa menjelaskan perbedaan antara atom unsur yang satu dengan atom unsur lainnya.
2. Teori Atom Thomson
Tahapan perkembangan Teori Atom selanjutnya adalah teori yang dikemukakan oleh Thomson. Teori ini muncul setelah teori Dalton. Dalam perkembangannya, Thomson melakukan perbaikan terkait kelemahan yang terdapat dalam teori yang dikemukakan oleh Dalton yang merupakan penemu pertama teori modern yang membahas tentang atom.
Dalam hal ini, perbaikan terkait Teori Atom yang dikemukakan oleh Dalton adalah dengan penemuan elektron oleh Thomson pada tahun 1897. Dalam hal ini, elektron merupakan partikel yang bermuatan negatif.
Penemuan yang dilakukan oleh Thomson ini diperoleh melalui sebuah percobaan dengan menggunakan tabung sinar katode. Berdasarkan percobaan tersebut, Thomson menyimpulkan bahwa sinar katode adalah sebuah partikel dikarenakan dapat memutar baling-baling yang diletakkan diantara anode dan katode.
Partikel tersebut merupakan partikel penyusun atom yang bermuatan negatif. Nah, inilah yang nantinya dalam Teori Atom versi Thomson disebut dengan elektron.
Isi dari Teori Atom yang dikemukakan oleh Thomson adalah atom merupakan sebuah bola pejal yang memiliki muatan positif. Selain itu, di dalamnya tersebar elektron yang memiliki muatan negatif. Teori yang dikemukakan oleh Thomson ini juga disebut dengan teori roti kismis. Hal ini dikarenakan kismis mewakili atom positif yang melekat pada roti sebagai elektron negatif.
Rincian Teori Atom yang dikemukakan oleh Thomson memiliki beberapa kelebihan dibandingkan dengan teori Dalton. Beberapa kelebihan dari teori ini adalah sebagai berikut:
- Detail Teori Atom dari Thomson membuktikan bahwa atom bukan merupakan bagian terkecil dari suatu unsur. Hal ini dikarenakan Thomson menemukan adanya partikel lain yang bermuatan negatif dan terdapat pada atom.
- Membuktikan bahwa atom bersifat netral yang tersusun dari partikel-partikel yang memiliki muatan positif dan negatif.
- Membuktikan bahwa adanya elektron dalam semua unsur benda.
Namun, Teori Atom yang dikemukakan oleh Thomson tersebut masih memiliki beberapa kekurangan. Adapun kekurangan dari teori ini adalah sebagai berikut:
- Tidak dapat menjelaskan tentang susunan muatan positif dan jumlah elektron yang terdapat dalam bola
- Tidak dapat menjelaskan tentang inti dari atom.
3. Teori Atom Rutherford
Perkembangan selanjutnya terkait Teori Atom adalah teori yang dikemukakan oleh Rutherford. Teori ini didasarkan pada eksperimen dengan melakukan penembakan partikel alfa terhadap lempeng emas. Eksperimen tersebut kemudian dikenal dengan eksperimen Geiger-Marsden.
Nama dari eksperimen tersebut merupakan murid dari Rutherford. Pada waktu itu, ia bersama kedua muridnya tersebut melakukan percobaan dengan menembakkan partikel atau sinar alfa terhadap lempeng tipis emas. Partikel alfa sendiri merupakan partikel yang memiliki muatan positif, bergerak lurus serta memiliki daya tembus yang besar.
Dari percobaan yang dilakukan tersebut, sinar alfa ada yang dibelokkan, dipantulkan dan diteruskan. Percobaan yang dilakukan tersebut sebenarnya ditujukan untuk membuktikan kebenaran Teori Atom Thomson di mana atom merupakan sebuah bola pejal yang bermuatan positif dan jika dikenai partikel alfa akan dipantulkan atau dibelokkan.
Hasil yang didapatkan dari percobaan tersebut kemudian dikembangkan menjadi sebuah hipotesis Teori Atom Rutherford yang menyatakan beberapa hal, diantaranya adalah sebagai berikut:
- Elektron yang memiliki muatan negatif bergerak mengelilingi inti atom yang bermuatan positif dengan kecepatan yang sangat tinggi
- Atom memiliki inti atom yang bermuatan positif dan menjadi pusat massa atom
- Penyebaran partikel alfa tidak dipengaruhi oleh adanya awan elektron
- Sebagian besar dari atom merupakan permukaan yang kosong atau hampa
- Sebagian kecil dari partikel alfa yang lewat akan dibelokkan dan sedikit sekali yang dipantulkan sedangkan sebagian besar lainnya tidak mengalami hambatan.
Pada tahun 1922, berdasarkan eksperimen yang dilakukan sebelumnya, Rutherford menyangkal Teori Atom yang dikemukakan oleh Thomson. Ia mengatakan bahwa atom memiliki inti yang merupakan pusat massa dan diberi nama nukleus yang dikelilingi oleh awan elektron yang bermuatan negatif.
Pernyataan ini kemudian dinamakan dengan Teori Atom Rutherford. Dalam perkembangannya, teori ini memiliki beberapa kelebihan, yaitu:
- Dapat menggambarkan serta menjelaskan bentuk lintasan elektron yang mengelilingi inti dari atom sehingga mudah dipahami
- Dapat memberikan kesimpulan bahwa atom tersusun dari inti serta elektron yang mengelilingi di mana satu sama lain terpisah oleh ruang hampa
- Dapat menjelaskan pergerakan elektron di sekitar atom.
Akan tetapi, Teori Atom yang dikemukakan oleh Rutherford tersebut masih memiliki beberapa kekurangan. Beberapa diantaranya adalah sebagai berikut:
- Tidak mampu menjelaskan kenapa elektron tidak pernah jatuh ke dalam inti atom sesuai dengan teori fisika klasik
- Tidak mampu menjelaskan terkait spektrum garis pada atom hidrogen
- Tidak mampu menjelaskan letak dari elektron dan cara rotasinya terkait inti atom
- Elektron yang bergerak akan memancarkan energi sehingga secara keseluruhan energi atom tidak stabil.
4. Teori Atom Bohr
Sekitar tahun 1913, seorang pakar fisika dari Denmark, yaitu Bohr melakukan eksperimen yang kemudian dikenal dengan nama spektrum atom hidrogen. Eksperimen yang dilakukan tersebut bertujuan untuk menyempurnakan capaian dalam Teori Atom Rutherford yang sudah muncul sebelumnya. Eksperimen ini berhasil menggambarkan keadaan elektron.
Penjelasan yang diberikan oleh Bohr mengenai atom hidrogen adalah gabungan dari teori klasik yang berasal dari Teori Atom Rutherford dan teori kuantum yang dijelaskan oleh Planck. Adapun hipotesis dari Bohr terkait hasil eksperimen yang dilakukan adalah sebagai berikut:
- Elektron dapat berpindah dari orbit satu ke orbit yang lain dengan dasar tingkatan energi. Elektron akan berpindah menuju ke orbit yang memiliki energi lebih tinggi jika elektron menyerap energi yang memiliki besaran sama dengan perbedaan energi antara dua orbit yang bersangkutan.
Sebaliknya, elektron yang berpindah ke orbit yang memiliki energi lebih rendah akan memancarkan radiasi yang teramati sebagai spektrum garis yang besarnya sama dengan perbedaan energi antara kedua orbit yang bersangkutan.
- Elektron akan berada dalam keadaan stationer dan tidak memancarkan energi selama dalam orbitnya.
- Jika elektron berpindah dan menempati orbit yang lebih tinggi, maka atom dalam molekul berada dalam tingkat tereksitasi.
- Jika elektron berpindah dan menempati orbit yang lebih rendah, maka atom dan molekul berada dalam tingkat dasar.
- Elektron mengelilingi inti atom dalam orbit tertentu yang berbentuk lingkaran dan disebut dengan kulit elektron di mana dinyatakan dalam bentuk notasi K, L, M, N dan seterusnya.
- Energi yang dimiliki elektron pada masing-masing orbit dapat mempengaruhi besar kecil lingkaran orbit.
Dalam hal ini, Teori Atom Bohr digambarkan seperti sebuah tata surya mini. Berdasarkan teori ini, maka elektron mengelilingi atom pada lintasan tertentu yang dinamakan dengan kulit elektron. Teori yang dikemukakan oleh Bohr ini memiliki beberapa kelebihan, yaitu:
- Dapat menjelaskan tentang spektrum atom hidrogen secara akurat
- Dapat membuktikan adanya lintasan elektron untuk atom hidrogen
- Dapat memperbaiki kelemahan dari Teori Atom yang dikemukakan oleh Rutherford.
Akan tetapi, Teori Atom yang dikemukakan oleh Bohr masih memiliki beberapa kekurangan. Adapun beberapa kekurangan yang dimaksud adalah sebagai berikut:
- Tidak banyak menjelaskan tentang spektrum warna dari atom yang memiliki banyak elektron atau yang lebih kompleks
- Tidak dapat menjelaskan tentang adanya garis halus dalam spektrum hidrogen karena elektron dianggap sebagai partikel
- Model atom Bohr memiliki nilai momentum sudut lintasan ground state yang salah
- Tidak bisa mengetahui intensitas relatif dari garis spektrum
- Tidak bisa menjelaskan atom selain atom hidrogen.
Teori Atom modern
Teori Atom berkembang lagi pada tahun 1924. Dalam hal ini ada tokoh Perancis bernama Louis de Broglie yang menyempurnakan kelemahan Teori Atom yang dikemukakan oleh Bohr. Ia menjelaskan bahwa elektron tidak hanya bersifat partikel, namun juga bisa bersifat gelombang.
Pendapat ini kemudian dikembangkan lagi oleh Edwin dan Werner dan melahirkan Teori Atom modern. Teori ini juga disebut dengan nama Teori Atom Mekanika Kuantum. Dasar dari teori ini adalah gerakan elektron dalam mengelilingi inti bersifat layaknya sebuah gelombang. Hingga saat ini, teori ini merupakan teori paling mutakhir terkait atom.
Demikian beberapa penjelasan mengenai kemunculan dan perkembangan dari Teori Atom. Teori ini merupakan salah satu yang paling penting dalam hal pemahaman mengenai benda-benda terkait ilmu fisika dan kimia. Semoga bermanfaat.
1 Komentar
Kirim Komentar
Baca Juga Yang Lainnya…
Mengenal Jurusan Silvikultur IPB, Fasilitas dan Faktanya yang Harus Kamu Ketahui
Jurusan silvikultur IPB menjadi jurusan pertama di Indonesia yang berfokus pada kehutanan. Yuk cari tau selengkapnya tentang jurusan ini!
Siap-Siap Daftar! Ini Jurusan Politeknik Negeri Semarang dan Akreditasinya
Politeknik Negeri Semarang memiliki banyak sekali pilihan jurusan dalam program vokasi dan Magister. Ini daftar jurusan Politeknik Negeri Semarang dan akreditasinya.
Jadi Kampus Bela Negara, Ini Daftar Jurusan yang Ada di UPN Jogja
UPN Veteran Yogyakarta menjadi salah satu kampus bela negara yang berada di bawah binaan Departemen Pertahanan RI. Apa saja jurusan yang ada di UPN Jogja ini?
Mau Jadi Dokter Sekaligus Belajar Agama? Ini 3 UIN yang Ada Jurusan Kedokteran
Banyak yang ingin menjadi dokter sekaligus belajar agama Islam. Berikut 3 pilihan UIN yang ada jurusan kedokteran.
5 Alasan Memilih Jurusan Psikologi yang Banyak Diminati Lulusan Baru
Jurusan psikologi jadi jurusan yang peminatnya cukup banyak setiap tahunnya. Berikut alasan memilih jurusan psikologi yang harus kamu pertimbangkan.

Sama-Sama dalam Aspek Hukum, Yuk Kenalan dengan Ilmu Kedokteran Forensik dan Medikolegal
Dunia kedokteran ada yang berkolaborasi dengan ilmu hukum, lho. Yuk kenalan dengan ilmu kedokteran forensik dan medikolegal!

Jangan Asal Pilih! Ini Manfaat Memilih Kampus TOP 10 untuk Masa Depan!
Menentukan perguruan tinggi terbaik di Indonesia bisa dilihat dari peringkat di Webometrics atau The WUR. Karena ada manfaat memilih kampus TOP 10 untuk masa depan.

Pendaftaran Taruna TNI 2024: Jadwal, Persyaratan dan Tahapan Pendaftaran
TNI RI segera kembali membuka pendaftaran untuk pangkat Taruna pada pertengahan Maret ini. Berikut jadwal, persyaratan dan tahapan pendaftaran Taruna TNI 2024.

Pendaftaran STMKG 2024: Prodi, Jadwal, Persyaratan dan Alur Pendaftarannya
Sekolah kedinasan di bawah naungan BMKG, yakni STMKG menjadi sekolah kedinasan iklim, atmosfer dan juga kebumian satu-satunya. Simak pendaftaran STMKG 2024 disini!

Siap-Siap! Ini Jadwal dan Persyaratan Pendaftaran Poltekip Poltekim 2024
Pendaftaran Poltekip dan Poltekim sebentar lagi akan dibuka. Cek informasi jadwal pendaftaran Poltekip Poltekim 2024 di sini!

Sudah Dibuka! Ini Informasi dan Jadwal Pendaftaran Tamtama TNI AD 2024
TNI AD membuka pendaftaran untuk golongan pangkat Tamtama tahun angkatan 2024. Simak jadwal dan informasi pendaftaran Tamtama TNI AD selengkapnya di sini!

9 Jurusan yang Hanya Ada Satu di Indonesia, Anti Mainstream!
Kamu mau lulus tapi bosan dengan jurusan yang itu-itu saja? Coba simak 9 jurusan yang hanya ada satu di Indonesia ini!

Informasi Beasiswa Kuliah, Pendaftaran Beasiswa Yasbil 2024
Kamu yang bercita-cita menjadi pendidik namun memiliki halangan karena faktor finansial untuk melanjutkan pendidikan, simak informasi beasiswa kuliah berikut dari Yasbil!

7 Fakta UPI yang Harus Kamu Tau, Semuanya Bikin Takjub!
Universitas Pendidikan Indonesia (UPI) dikenal sebagai kampus pendidikan yang jadi favorit banyak orang. Coba cek fakta UPI berikut, yuk!










Terima Kasih kak, sangat bermanfaat 🙏